الطاقة في التفاعلات الكيميائية ⚡🌡️
الطاقة: المحرك الخفي
تستطيع التفاعلات الكيميائية امتصاص أو تحرير أنواع عديدة من الطاقة، مثل: الكهربائية، الضوئية، الصوتية، والحرارية.
📥 امتصاص الطاقة
تحتاج بعض التفاعلات إلى تزويدها بطاقة (مثل الكهرباء لكسر جزيئات الماء) لتكوين النواتج.
📤 تحرير الطاقة
تتحرر الطاقة عند تكوين روابط جديدة أكثر استقراراً في النواتج، مثل حرارة مشعل اللحام.
ماص أم طارد للحرارة؟
عندما يتعلق الأمر بالحرارة (Therm)، نستخدم مصطلحين أساسيين:
❄️ تفاعل ماص للحرارة (Endothermic):
يمتص الطاقة الحرارية من البيئة المحيطة.
مثال: الكمادات الباردة التي تمتص الحرارة من جلد الشخص المصاب.
🔥 تفاعل طارد للحرارة (Exothermic):
يحرر طاقة حرارية إلى البيئة المحيطة.
مثال: عمليات الاحتراق التي تنتج حرارة وضوءاً.
تحرير سريع أم بطيء؟
لا تنطلق الحرارة دائماً بنفس السرعة، ولدينا نوعان:
تحرير سريع
مثل احتراق البنزين في المحركات أو لهب مشعل اللحام.
تحرير بطيء
مثل صدأ الحديد، حيث تنطلق الحرارة ببطء فلا نشعر بها.
موقع كلمة "طاقة" في المعادلة
يساعدنا موقع كلمة "طاقة" في المعادلة على معرفة نوع التفاعل:
1. مع المتفاعلات:

كتابة الطاقة مع المتفاعلات تدل على أنها مكون ضروري لحدوث التفاعل (ماص).
2. مع النواتج:
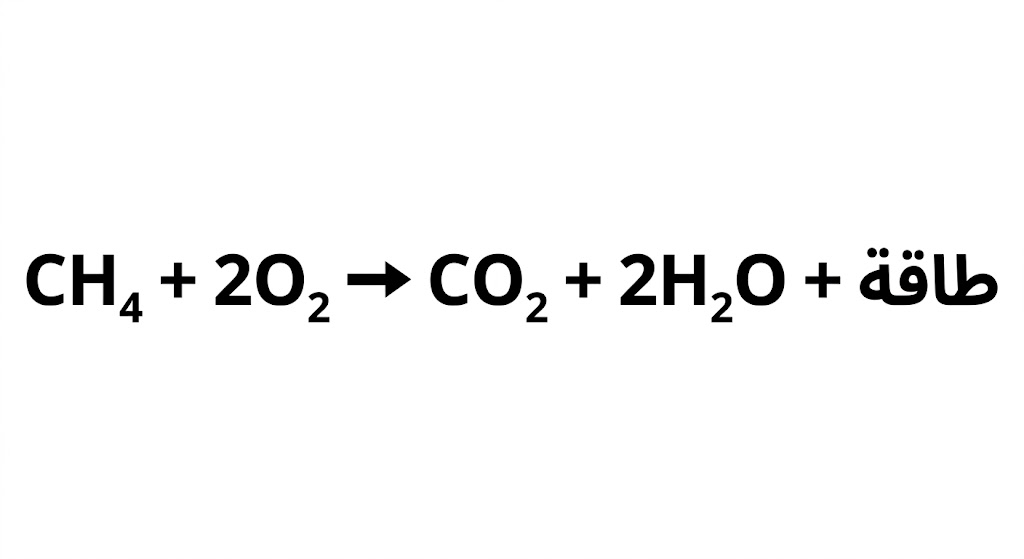
كتابة الطاقة مع النواتج تدل على تحررها كناتج من نواتج التفاعل (طارد).
ملخص الطاقة الكيميائية
- تغير الطاقة: كل تفاعل يصاحبه امتصاص أو تحرير للطاقة.
- تفاعل ماص للحرارة: يمتص الحرارة من المحيط (مثل الكمادات الباردة).
- تفاعل طارد للحرارة: يحرر الحرارة إلى المحيط (مثل الاحتراق).
- سرعة تحرير الطاقة: قد يكون التحرير سريعاً كالانفجار أو بطيئاً كالصدأ.
- موقع الطاقة في المعادلة: يحدد إذا كان التفاعل يحتاج طاقة (متفاعلات) أو ينتجها (نواتج).
أحسنت يا مهندس الطاقة!
لقد أتقنت فهم كيفية انتقال الطاقة في التفاعلات الكيميائية. أنت مستعد الآن للدروس القادمة!

