الفصل الثامن - الدرس الخامس
الرابطة التساهمية والقطبية 🤝🧪
التشارك هو السر
بعض الذرات يصعب عليها فقد أو اكتساب عدد كبير من الإلكترونات. بدلاً من ذلك، تقوم بالمشاركة بإلكتروناتها مع ذرات لافلزية أخرى.

تتحرك الإلكترونات المشتركة بين مستويات الطاقة الخارجية للذرتين، مما يجعل غلاف كل منهما مكتملاً ومستقراً. تسمى الجسيمات المتعادلة الناتجة عن هذا التشارك الجزيئات.
سؤال: ما هو الفرق الجوهري بين الرابطة الأيونية والتساهمية؟
أنواع الروابط التساهمية
لا تشارك الذرة دائماً بنفس العدد من الإلكترونات؛ فهناك ثلاث درجات من التشارك:
- ☝️ الرابطة الأحادية: تشارك كل ذرة بإلكترون واحد (زوج واحد من الإلكترونات).
- ✌️ الرابطة الثنائية: تشارك كل ذرة بإلكترونين (زوجان من الإلكترونات).
- 🤟 الرابطة الثلاثية: تشارك كل ذرة بثلاثة إلكترونات (ثلاثة أزواج من الإلكترونات).
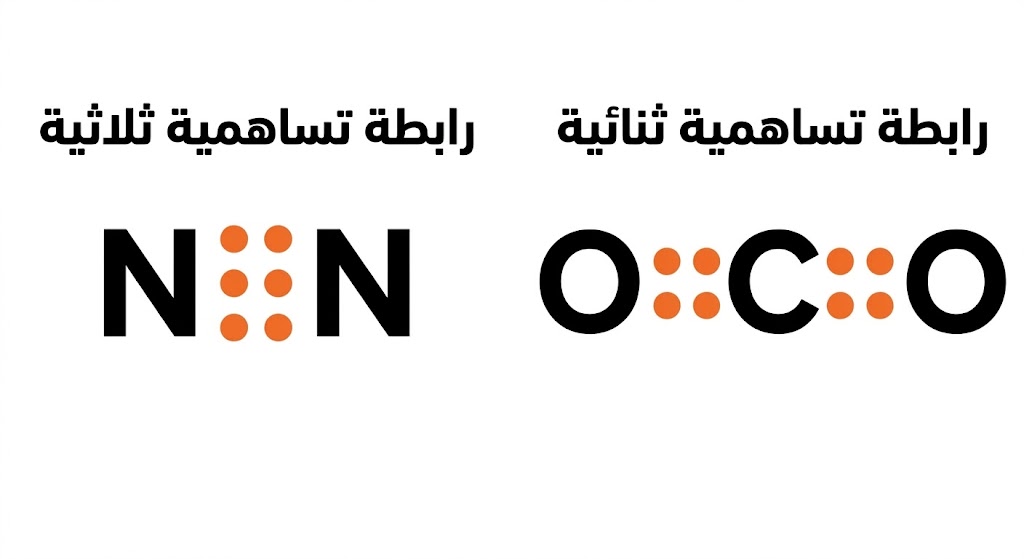
سؤال: كم زوجاً من الإلكترونات يتم مشاركته في الرابطة الثلاثية؟
القطبية: لعبة شد الحبل
هل تتشارك الذرات دائماً بالتساوي؟ الجواب: لا. بعض الذرات تجذب الإلكترونات نحوها بقوة أكبر، مما يخلق أقطاباً كالمغناطيس:
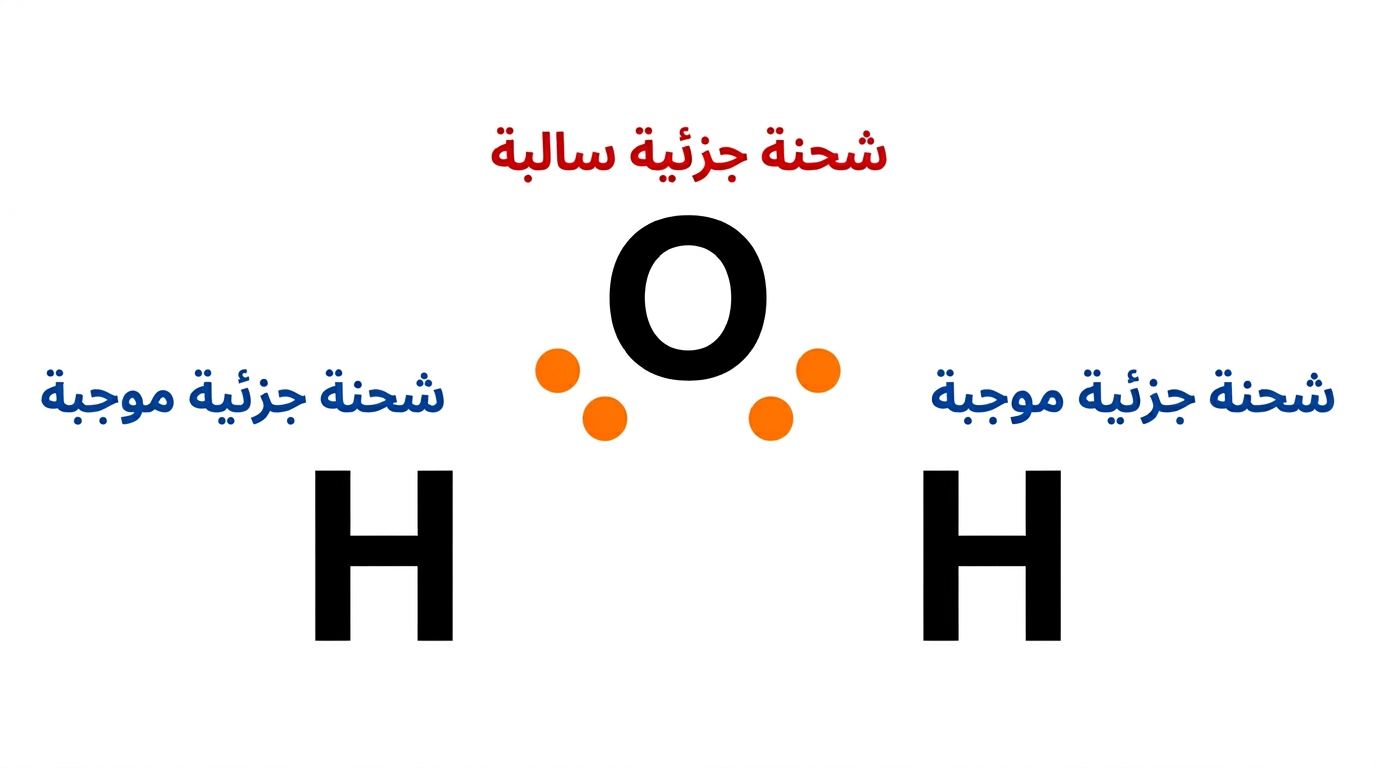
- 💧 الجزيئات القطبية: مشاركة غير متساوية، كما في جزيء الماء (H₂O) وكلوريد الهيدروجين (HCl)، حيث تجذب الذرة الأقوى الإلكترونات أكثر.
- 🎈 تجربة انحراف الماء: لأن الماء (H₂O) قطبي، ينحرف مساره عند تقريب بالون مشحون منه.
- 🚫 الجزيئات غير القطبية: مشاركة متساوية تماماً، كما في جزيء النيتروجين (N₂) أو الهيدروجين (H₂).
خاتمة الفصل الثامن
- 🤝 التساهمية: تشارك لافلزات بالإلكترونات لتكوين جزيئات متعادلة.
- ⚡ القطبية: تحدث عندما تجذب ذرة الإلكترونات بقوة أكبر من جارتها.
- 💎 الاستقرار: هو الهدف دائماً، سواء بالفقد أو الاكتساب أو التشارك.
🏆🧪✨
ألف مبروك يا بطل!
لقد أتممت دراسة الفصل الثامن بنجاح، وأصبحت خبيراً في أسرار الذرات وروابطها.

