الرابطة الأيونية والفلزية 🤝⚡
الأيونات: ذرات فقدت توازنها
الذرة التي تفقد أو تكتسب إلكتروناً لم تعد ذرة متعادلة، بل تسمى أيوناً.
- فقد إلكترون (سالب) ⬅️ يصبح الأيون موجباً.
- اكتساب إلكترون (سالب) ⬅️ يصبح الأيون سالباً.
الرابطة الأيونية: قوة الجذب الكهربائي
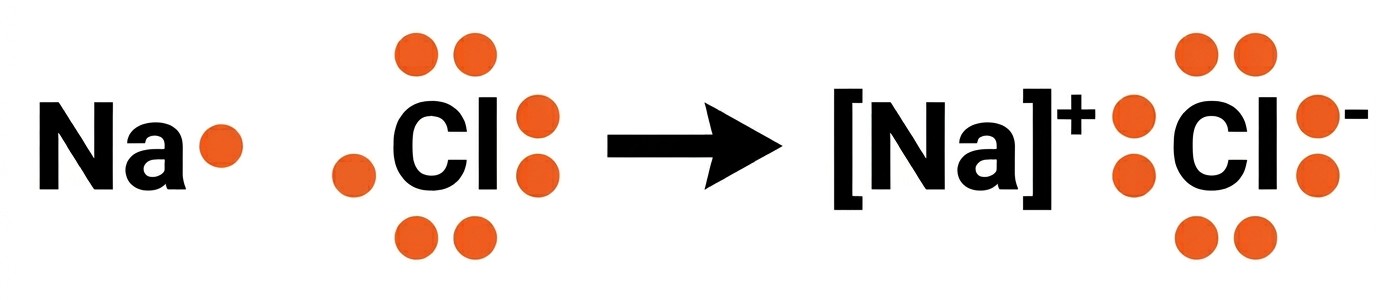
عندما تفقد ذرة (مثل الصوديوم) إلكتروناً وتكتسبه ذرة أخرى (مثل الكلور)، ينشأ تجاذب شديد بين الأيون الموجب والسالب. هذا التجاذب هو ما نسميه الرابطة الأيونية.
ينتج عن هذا الارتباط مركب مثل ملح الطعام (كلوريد الصوديوم). وتذكر أن بعض الذرات كالأكسجين والماغنيسيوم قد تتبادل إلكترونين لتصل للاستقرار.
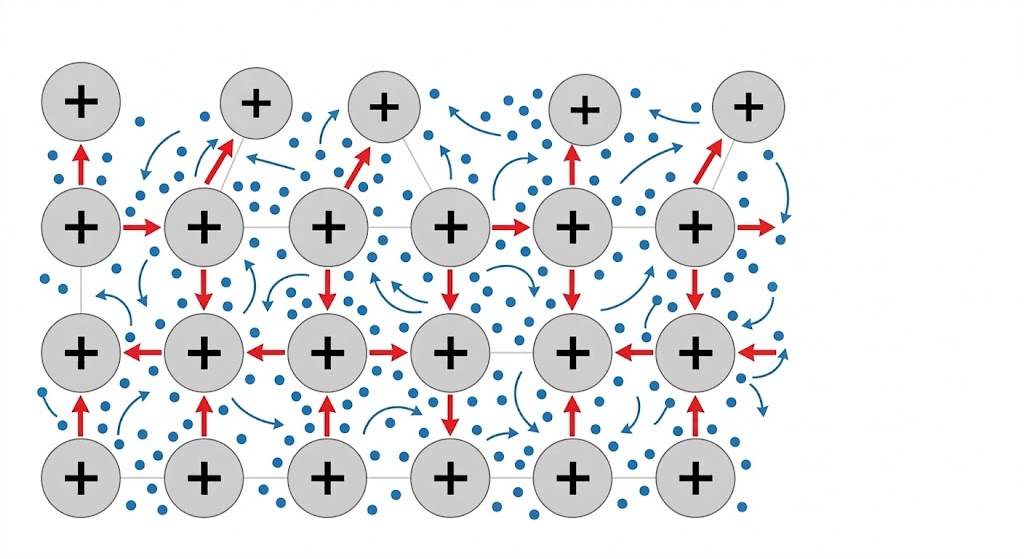
الرابطة الفلزية: بحر الإلكترونات
في الفلزات (كالفضة والحديد)، تتحرك إلكترونات المستوى الخارجي بحرية تامة بين الذرات، مما يشبه بحر الشحنات.
هذه الرابطة هي السر وراء خصائص الفلزات:
- 💡 التوصيل الكهربائي: بسبب حركة الإلكترونات الحرة من ذرة لأخرى.
- 🔨 القابلية للطرق والسحب: الطبقات تنزلق فوق بعضها دون أن تنكسر بفضل تجمع الإلكترونات المشترك.
ملخص الدرس
- ➕ الأيون الموجب: ذرة فقدت إلكتروناً.
- ➖ الأيون السالب: ذرة اكتسبت إلكتروناً.
- 🧲 الرابطة الأيونية: تجاذب بين أيونات موجبة وسالبة.
- 🌊 الرابطة الفلزية: تجاذب ناتج عن حركة الإلكترونات الحرة (بحر الإلكترونات).
أحسنت يا بطل العلوم!
لقد فهمت الآن كيف تترابط ذرات الفلزات والأملاح لتكون العالم من حولنا.

