المجموعات والتوزيع الإلكتروني 🧪💎
الغازات النبيلة: ملوك الاستقرار
عناصر المجموعة 18 (مثل الهيليوم، النيون، الأرجون) هي أكثر العناصر استقراراً؛ لأن مستوى طاقتها الخارجي مكتمل بـ 8 إلكترونات (أو 2 للهيليوم).
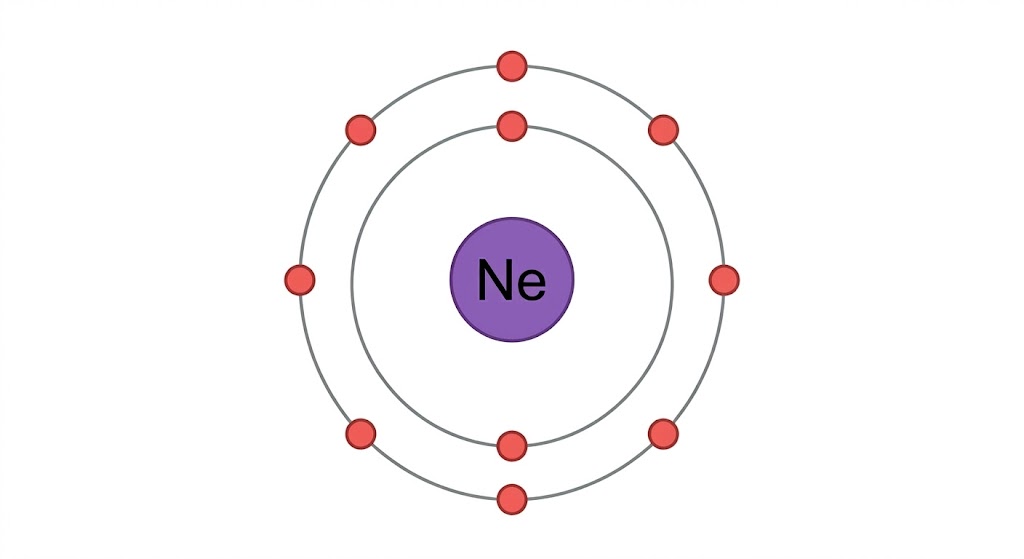
بسبب استقرارها العالي، فهي لا تتحد بسهولة مع العناصر الأخرى، وتستخدم في حماية أسلاك المصابيح واللوحات الإعلانية الملونة. وكانت تُعرف قديما بالغازات الخاملة لأنهم كانوا يظنون أنها لا تتفاعل إطلاقاً.
الهالوجينات: الطامعة في الإلكترون
عناصر المجموعة 17 (مثل الفلور والكلور) لها 7 إلكترونات في مستواها الخارجي، لذا فهي تحتاج لإلكترون واحد فقط لتستقر.
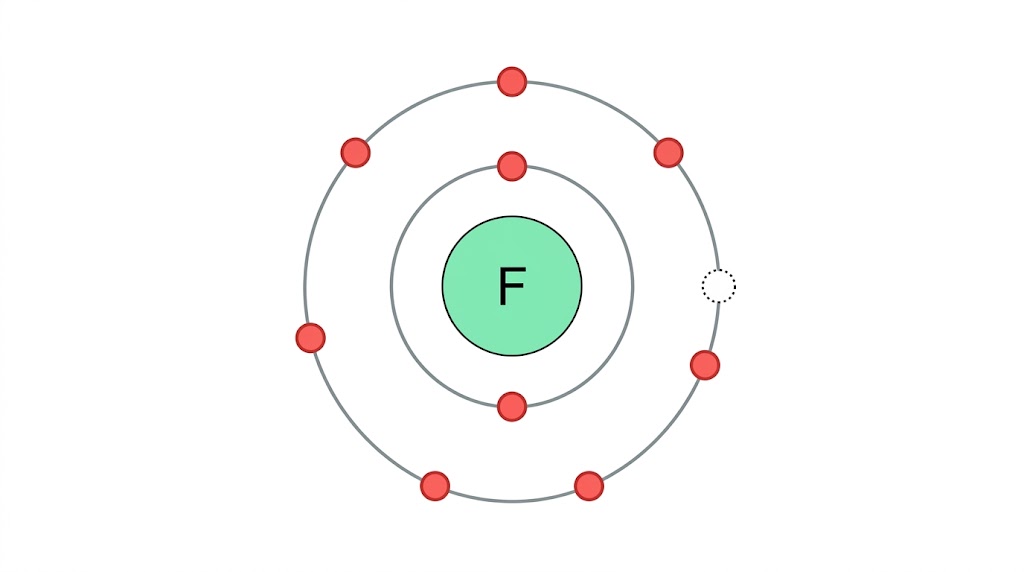
الفلزات القلوية: الكريمة بإلكترونها
عناصر المجموعة 1 (مثل الصوديوم والبوتاسيوم) لها إلكترون واحد فقط في مستواها الخارجي. هي تفضل فقد هذا الإلكترون لتصل للاستقرار.
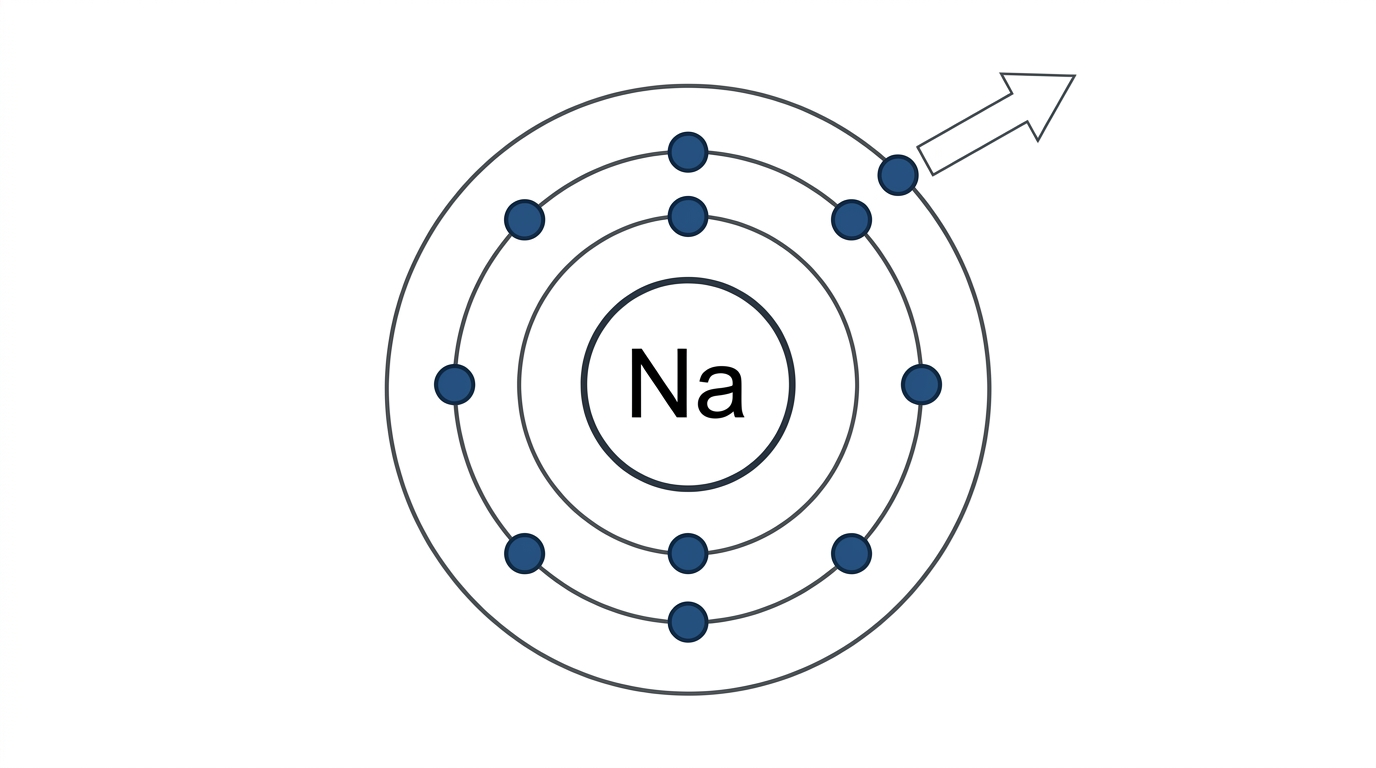
ملخص المجموعات
- 💎 الغازات النبيلة (18): مستقرة جداً (المستوى الخارجي مكتمل بـ 8) ما عدا الهيليوم مستقر بإلكترونين.
- 💥 الهالوجينات (17): نشطة جداً (تحتاج 1 إلكترون)، يزداد نشاطها كلما اتجهنا لأعلى.
- ⚡ الفلزات القلوية (1): نشطة جداً (تفقد 1 إلكترون)، يزداد نشاطها كلما اتجهنا لأسفل.
خبير كيميائي متميز!
لقد أتقنت فهم العلاقة بين توزيع الإلكترونات ونشاط المجموعات.

