التوزيع الإلكتروني في الذرة
مكونات الذرة
- البروتونات: جسيمات موجبة الشحنة موجودة في النواة.
- النيوترونات: جسيمات متعادلة الشحنة موجودة في النواة.
- الإلكترونات: جسيمات سالبة الشحنة تدور حول النواة.
نموذج الذرة: ذرة الليثيوم
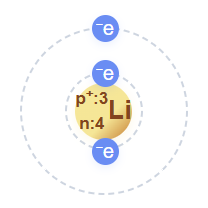
ذرة الليثيوم تتكون من 3 بروتونات و4 نيوترونات في النواة، و3 إلكترونات تدور حولها موزعة على مستويين للطاقة.
التوزيع الإلكتروني: 2 إلكترون في المستوى الأول و1 إلكترون في المستوى الثاني.
التوزيع الإلكتروني: 2 إلكترون في المستوى الأول و1 إلكترون في المستوى الثاني.
مستويات الطاقة
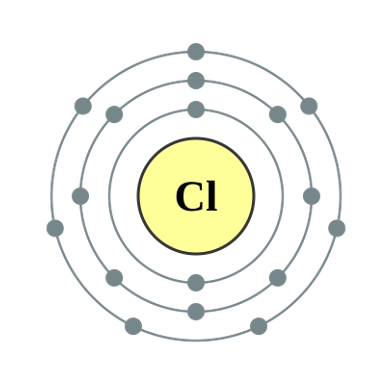 تتحرك الإلكترونات في مساحات حول النواة ولا يمكن تحديد مساراتها بدقة.
تتحرك الإلكترونات في مساحات حول النواة ولا يمكن تحديد مساراتها بدقة.
- المستوى الأول: يتسع لعدد 2 إلكترون
- المستوى الثاني: يتسع لعدد 8 إلكترونات
- المستوى الثالث: يتسع لعدد 18 إلكترون
- المستوى الرابع: يتسع لعدد 32 إلكترون
التوزيع الإلكتروني
- المستوى الأول يستقر عندما يحتوي على 2 إلكترون.
- المستوى الثاني يستقر عندما يحتوي على 8 إلكترونات.
- المستوى الثالث يستقر عندما يحتوي على 8 إلكترونات (بشكل أفضل من 18 إلكترون).
أهمية التوزيع الإلكتروني
التوزيع الإلكتروني ليس مجرد أرقام، بل هو الذي يحدد شخصية العنصر الكيميائية، وكيف سيتفاعل مع العناصر الأخرى لتكوين المركبات.
لعبة التوزيع الإلكتروني
أدخل عدد الإلكترونات (من 1 إلى 20) لتتعرف على التوزيع الصحيح:
اختبر فهمك
1. ما هو التوزيع الإلكتروني الصحيح لذرة الصوديوم (Na) التي تحتوي على 11 إلكترونًا؟
2. كم عدد إلكترونات مستوى الطاقة الأخير لذرة الأكسجين (O) التي تحتوي على 8 إلكترونات؟
3. أي من العناصر التالية لديه مستوى طاقة أخير مكتمل (مستقر)؟

